Anggap suatu elektron bermassa me bergerak dalam suatu orbit berjari-jari r dengan frekuensi f. Momentum sudut elektron ini adalah L = mevr = meωr2 = 2meπfr2.
Gerakan elektron inilah menimbulkan arus. Arus didefinisikan sebagai
banyaknya muatan yang mengalir tiap detik, jadi arus yang disebabkan
oleh gerakan elektron ini sama dengan I = qf = -ef. Gerakan elektron ini
juga menimbulkan medan magnet (ingat partikel bermuatan yang beregrak
akan menimbulkan medan magnetik). Jika elektron ini diberi medan
magnetik (kita namakan medan magnetik luar), B (misalnya berarah sejajar sumbu z) akan memberikan torsi yang akan mengubah arah gerakan elektron. Besarnya Torsi, (τ), akibat medan magnetik ini diberikan oleh rumus:
τ = μ X B
μ adalah suatu besaran yang dinamakan momen magnetik,
besarnya μ = IA. Arah momen magnetik sama dengan arah momentum sudut
untuk partikel yang bermuatan positif (gambar 1b) dan berlawanan dengan
arah momentum sudut untuk partikel yang bermuatan negatif (gambar 1c).
 |
| Gambar 1 |
A adalah luar dari bidang orbit. Dengan menggunakan nilai I dan A = πr2, kita peroleh;
Jadi, besarnya torsi yang disebabkan oleh medan B (2)
Torsi inilah yang memutar orbit elektron (gambar 2a).
Berapa besar energi magnetik yang dapat diserap oleh elektron??
Energi yang diberikan oleh medan magnetik adalah
Di mana θ adalah sudut antara medan magnetik B dan momen magnetik μ. Besaran dalam kurung (-e/(2me ) dinamakan ratio giromagnetik (gyromagnetic ratio). Sekarang perhatikan gambar 2b. Dari gambar terlihat bahwa cos θ = mlℏ/L sehingga kita peroleh:
E = μB cos θ = (–e/2me)LB cos θ
Atau
Misalnya untuk l = 1, kita mempunyai ml = 1, 0 dan -1. Energi elektron yang semula besarnya E0 sekarang berubah menjadi:
Jadi ada tiga kemungkinan nilai energi yang dimiliki oleh elektron
(tingkat energi elektron sekarang pecah menjadi 3 bagian). Untuk l = 2
energi elektron akan pecah menjadi 5 bagian (sesuai dengan ml). Dari sini kita lihat pentingnya gerak orbit elektron. Juga kita lihat berapa eratnya hubungan antara ml dengan medan magnetik. Itulah sebabnya ml dinamakan bilangan kuantum magnetik.
 |
| Gambar 3 |
Pecahnya tingkat energi ini telah dibuktikan secara eksperimen oleh
Zeeman. Garis spektrum yang semula 1 pecah menjadi beberapa bagian
ketika atom hidrogen diberi medan magnetik kuat. Pecahnya garis spektrum
ini ternyata merupakan akibat transisi dari tingkat energi yang
terpecah itu (lihat gambar 3).
 |
| Gambar 4 |
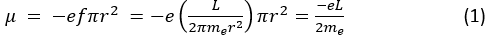




Post a Comment for "Efek Zeeman"
Sobat Fisika! Berikan Komentar di kolom komentar dengan bahasa yang sopan dan sesuai isi konten...Terimasih untuk kunjunganmu di blog ini, semoga bermanfaat!